长春应化所在血管阻断剂纳米药物研究中取得进展
肿瘤缺氧是人以及动物实体瘤的共同特征之一,可作为一个有效的治疗靶点。乏氧敏感前体药物具有选择性杀伤缺氧细胞的潜能,从而将肿瘤缺氧由一个劣势转化为选择性治疗的优势。然而,肿瘤内缺氧程度不足会导致药物失效。因此,如果能够选择性地提高肿瘤缺氧程度,将为基于乏氧敏感前体药物的策略提供有效性支持。
近年来,中国科学院长春应用化学研究所陈学思研究员和汤朝晖研究员研究团队致力于研究血管阻断剂纳米药物,特别是聚(L-谷氨酸)接枝聚(乙二醇)单甲醚/康普瑞汀(PLG-g-mPEG/CA4, CA4-NPs)。CA4是一种代表性的血管阻断剂,该研究团队之前研究证实了CA4-NPs静脉给药后主要分布在实体瘤的肿瘤血管周围,能够选择性破坏肿瘤血管(Acta Biomater, 2017, 53, 179)。近日报道了利用CA4-NPs选择性增加肿瘤区域缺氧,增效乏氧敏感前体药物TPZ(替拉扎明),用于转移性乳腺癌(4T1肿瘤模型)的治疗(Adv Mater, 2019, 31, 1805955)。该研究团队利用小鼠活体光声成像、肿瘤组织缺氧免疫荧光染色和缺氧诱导因子-1α(HIF-1α)三种手段验证了CA4-NPs能够诱导肿瘤乏氧。对于4T1荷瘤小鼠,起始肿瘤体积为180mm3时,大剂量的CA4-NPs联合TPZ治疗,可以实现肿瘤的完全抑制;起始体积为500mm3时,一次给药即可以使得肿瘤皱缩到140mm3。该研究说明,血管阻断剂纳米药物治疗可以选择性地增加肿瘤部位缺氧程度,从而使乏氧敏感前体药物发挥更强药效,血管阻断剂和乏氧敏感前体药物的联合治疗在实体肿瘤临床治疗方面具有应用前景。
另外,该研究团队在血管阻断剂纳米药物的宿主反应方面也取得了进展。基于CA4-NPs能选择性调控血管内皮生长因子A(VEGF-A)的表达,创新地采用CA4-NPs联合索拉菲尼在肝癌治疗上取得了显著的抑瘤效果(Acta Biomater, 2019, 92, 229)。该研究团队发现CA4-NPs能够引发肿瘤免疫抑制的微环境,诱导肿瘤内巨噬细胞向M2型转化,加入PI3Kγ抑制剂能够降低肿瘤内M2型肿瘤相关巨噬细胞的数量,使得CA4-NPs和PI3Kγ抑制剂发挥协同抗肿瘤作用(Adv Sci, 2019, 6, 1900327)。
该系列工作指出了血管阻断剂纳米药物具有高肿瘤血管靶向性,并与乏氧敏感前体药物、血管新生抑制剂以及PI3Kγ抑制剂有协同抗肿瘤作用,这为CA4-NPs的临床转化打下了理论基础。该系列工作得到国家自然科学基金委、科技部和中国科学院项目的支持。
(中国科学院生态环境高分子材料重点实验室)
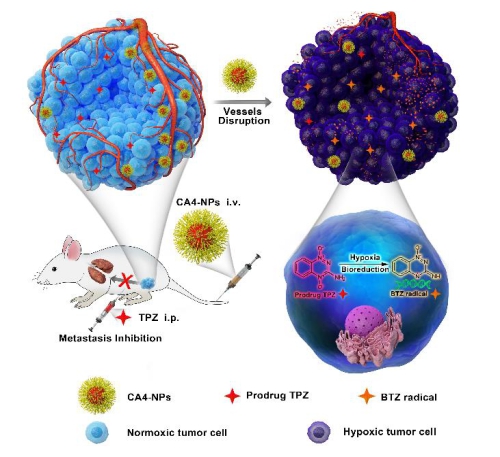
CA4-NPs诱导肿瘤缺氧增效TPZ的治疗效果示意图



